1er août 2025
 3 min
3 min
Bienvenue sur LeFil.vet
L'accès au site web nécessite d'être identifié.
Merci de saisir vos identifiants de connexion.
Indiquez votre email dans le champ ci-dessous.
Vous recevrez un email avec vos identifiants de connexion.

16 juin 2020
Trois voies pour la thérapeutique de la péritonite infectieuse féline
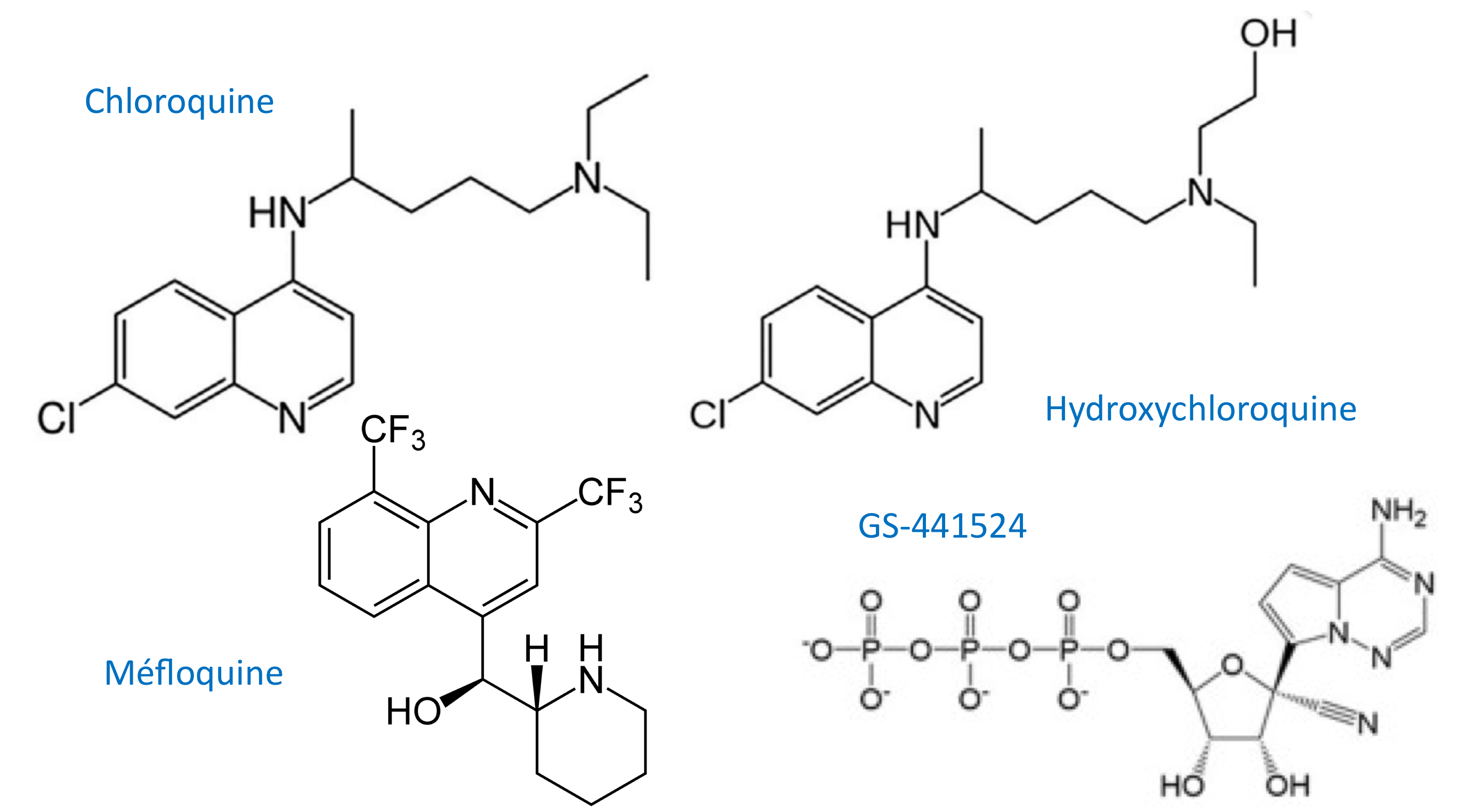
Deux articles scientifiques viennent d'être publiés qui explorent, à leur tour, l'effet potentiel de composés proches de la chloroquine sur un coronavirus… Mais il s'agit du virus plus purement félin de la péritonite infectieuse (PIF) et non de celui de la Covid-19. Un troisième article fournit des résultats complémentaires à ceux présentés en 2019 sur un antiviral initalement développé contre le virus du SARS (de 2003), et qui est utilisé en essai clinique contre la PIF aux USA.
Les travaux in vitro ont été conduits par une équipe de virologistes et chimistes japonais (faculté vétérinaire de l'université Kitasato, à Aomori), qui avait déjà exploré l'effet de la chloroquine sur le virus de la PIF dès 2013. A l'époque, ces auteurs avaient travaillé in vitro avec de la chloroquine (CQ) sur des cellules embryonnaires de chat et sur des monocytes (cellules progénitrices des macrophages) extraites de chats EOPS. Dans les deux lignées, ils avaient obtenu un effet antiviral (réduction de la réplication), mais plus marqué lorsque la CQ était présente dans le milieu de culture avant le virus. Ils avaient alors jugé ces résultats suffisants pour passer à l'in vivo, sur des chats EOPS inoculés avec le virus (voie orale) :
Si des différences numériques en faveur des groupes traités avec la CQ sont apparues pour plusieurs paramètres, aucune différence significative n'avait été observée entre groupes pour aucun paramètre et tous les chats inoculés sont morts d'infection clinique, avec une durée moyenne de survie allant de 34,3 à 21 jours pour les premier et dernier groupes.
Le feuilleton médiatique sur l'hydroxychloroquine (HCQ) lancé par la Covid-19 a sans doute remonté le dossier correspondant sur le bureau de ces virologues vétérinaires car ils viennent de publier un nouvel essai, in vitro seulement cette fois. Ils associent CQ ou HCQ et interféron oméga félin recombinant (la spécialité autorisée au Japon) contre le virus de la PIF (sérotype I ou II) dans la même lignée de cellules embryonnaires félines que précédemment. Ils montrent que la cytotoxicité de la HCQ est plus limitée que celle de la CQ, pour un effet antiviral comparable. Ils ont donc utilisé la HCQ (100 µM) en association avec l'IFN-omega (104 UI/ml), toujours en culture. Ils observent, lorsque les deux composés sont présents dans le milieu avant le virus :
Lorsque les composés sont placés dans le milieu de culture 1 h après le virus, l'effet reste significatif sur la réplication (p<0,01) pour les trois souches de sérotype I testées (pas de résultat présenté pour le sérotype II). Ces auteurs estiment à nouveau que leurs éléments devraient justifier le passage à une expérimentation in vivo, mais ne permettent en rien de présumer de son succès. Ils estiment également nécessaire de réaliser une étude de pharmacocinétique/pharmacodynamie de l'hydroxychloroquine et de l'IFN-omega chez le chat.
C'est justement ce par quoi vient de commencer une équipe australienne (faculté vétérinaire de l'université de Sydney), qui a travaillé sur un autre composé antipaludéen de la même famille : la méfloquine (MFQ). Là encore, les essais in vitro de cette molécule d'humaine sur le virus de la PIF avaient été publiés antérieurement (en 2014) et montraitent une très faible cytotoxicité et une efficacité antivirale à faible dose. La présente étude vise « un traitement potentiel de la PIF », voire « des infections à calicivirus ». Ils ont donc administré à 7 chats adultes en bonne santé de la méfloquine, à la dose de 62,5 mg par voie orale, à quatre reprises (J0, J4, J7 et J10). Ils ont suivi la concentration plasmatique en MFQ (Cmax : 2,71 µg/ml et Tmax : 15 h). Le pic plasmatique est plus élevé quand la MFQ est administrée avec l'aliment, et la demi-vie est de 224,2 h (9,3 j). Lorsqu'elle est administrée en dehors des repas, la méfloquine peut provoquer « des vomissements chez certains chats » (un chat a vomi à la suite de deux administrations et a été retiré de l'étude). Elle s'accompagne d'une « légère augmentation de la concentration en diméthylarginine symétrique sérique (SDMA), mais pas en créatinine ». La concentration en SDMA augmente de manière significative à 168 et 366 h, et atteint alors (pour sa valeur médiane) la valeur supérieure de l'intervalle de référence (14 µg/dl), mais les auteurs hésitent à attribuer cet effet à la méfloquine plutôt qu'à l'anesthésie générale, pratiquée ici pour chaque prise de sang. Aucune modification hématologique n'étant notée. Pour avoir une idée de l'efficacité de la MFQ dans la PIF, « il y a besoin d'un essai clinique », car in vitro, une « inhibition marquée » de la réplication virale est publiée pour 10 µM, soit 3,78 µg/ml. Or la Cmax obtenue ici est inférieure, mais la concentration plasmatique moyenne est plus élevée (4,06 µg/ml) lors d'absorption avec l'aliment. Les auteurs espèrent aussi pouvoir conduire un essai de pharmacocinétique sur des chats atteints de PIF…
Enfin, l'équipe de la faculté vétérinaire d'UC Davis (USA) a publié un court rapport sur les résultats du traitement de quatre chats à PIF avec atteinte nerveuse par l'analogue de nucléosides GS-441524. Le bilan favorable d'un premier essai sur 18 chats PIF+ avait été publié l'an passé par cette équipe (voir LeFil du 15 février 2019). Dans le cas présent, les auteurs rapportent une rémission pour trois des quatre chats, dont deux au-delà d'un an après le début du traitement. Ils précisent que le composé « n'est pas disponible pour une utilisation routinière en clinique ».
Cette dernière publication porte à 22 le nombre de cas de PIF pour lesquels les données relatives à un traitement par le GS-441524 sont publiées. Les auteurs concluent que « des études pharmacocinétiques chez des chats sains et infectés, présentant une barrière hémato-encéphalique intacte ou endommagée seront nécessaires pour mieux définir la posologie optimale du GS-441524 chez les chats présentant une forme neurologique de PIF ».
1er août 2025
 3 min
3 min

31 juillet 2025
 5 min
5 min
29 juillet 2025
 6 min
6 min

28 juillet 2025
 4 min
4 min

25 juillet 2025
 5 min
5 min

24 juillet 2025
 4 min
4 min