9 mai 2025
 5 min
5 min
Bienvenue sur LeFil.vet
L'accès au site web nécessite d'être identifié.
Merci de saisir vos identifiants de connexion.
Indiquez votre email dans le champ ci-dessous.
Vous recevrez un email avec vos identifiants de connexion.

13 novembre 2023
Physiopathologie, diagnostic, traitement : le consensus de l'ACVIM sur les leptospiroses

Six experts en médecine vétérinaire, en médecine humaine et en santé publique ont fait le point sur les nouveautés relatives à la physiopathologie, au diagnostic et au traitement de la leptospirose chez le chien et le chat. L'objectif de ce groupe de travail de l'ACVIM (American College of Veterinary Internal Medicine) était de faciliter la prise en charge de cette affection par les praticiens. Ses conclusions ont été publiées en octobre dernier dans le Journal of Veterinary Internal Medecine.
Près de 300 sérovars de leptospires pathogènes ont été dénombrés à ce jour. Ils sont classés en sérogroupes, en fonction de leurs antigènes de surface. Cette classification est toutefois source de confusion, puisque des leptospires d'un même sérogroupe peuvent en fait appartenir à des espèces différentes. Pour plus de clarté, la taxonomie des leptospires a récemment été réorganisée en fonction du séquençage de leur ADN : 68 espèces de Leptospira ont ainsi été classées en deux sous-groupes pathogènes, P1 (les plus virulentes) et P2, et en deux sous-groupes saprophytes, S1 et S2.
Les rongeurs constituent le principal réservoir de la bactérie. L'environnement est la principale source de contamination, les leptospires pouvant persister dans le sol ou dans l'eau durant des semaines, voire des mois. Une contamination directe par contact avec un rongeur, voire un autre chien, est également possible, y compris en zone urbaine (prédation, morsure…). Si les chats peuvent être contaminés par Leptospira sp., ils sont habituellement considérés comme résistants à la maladie. L'ACVIM recommande toutefois d'envisager une leptospirose dans l'espèce féline en cas d'insuffisance rénale aiguë (IRA), en l'absence de toute autre cause identifiable et en présence de signes d'une infection systémique.
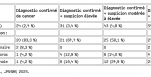
Généralement, la phase fébrile initiale n'est pas spécifique de la maladie. Bien que les manifestations cliniques qui apparaissent ensuite soient le plus souvent le reflet d'une néphrite tubulo-interstitielle aiguë et/ou, plus rarement, d'une atteinte hépatique associée, la maladie est en fait systémique. D'autres organes peuvent donc être atteints, y compris les poumons. Chez le chien, les symptômes les plus fréquents de la leptospirose d'après l'ACVIM sont :
Parce que l'IRA peut progresser très rapidement, l'ACVIM recommande d'envisager systématiquement la leptospirose en cas de syndrome fébrile aigu, surtout chez un chien qui n'est pas correctement vacciné.
En cas de leptospirose, les modifications de la formule sanguine le plus souvent observées sont une hausse des neutrophiles, une lymphopénie, une monocytose, une thrombocytopénie et une anémie non-régénérative modérée. L'hémostase est souvent anormale (jusqu'à 83 % des cas). Une coagulation intra-vasculaire disséminée (CIVD) est plus rarement observée. Au niveau biochimique, les anomalies vont refléter l'atteinte des différents organes : insuffisance rénale, insuffisance hépatique… Au niveau urinaire, glucosurie rénale et cylindrurie sont de bons indicateurs des lésions tubulaires. Une protéinurie est aussi observée dans la plupart des cas. Enfin, une radiographie thoracique est recommandée en cas de suspicion de leptospirose, même en l'absence de signes respiratoires. Cet examen mettra en évidence un éventuel syndrome hémorragique pulmonaire.
Les tests diagnostiques de leptospirose ayant tous leurs limites, il faudra souvent les combiner. La détection par un laboratoire des anticorps sériques dirigés contre les leptospires est une technique de choix en santé animale. Elle possède toutefois des limites en cas de contamination récente, puisque les anticorps peuvent ne pas avoir eu le temps d'être produits (phase précoce d'une maladie aiguë). Un test négatif isolé ne suffit donc pas à exclure une leptospirose. Dans ce cas, il est recommandé de renouveler le test, dans un délai de 7 à 14 jours. À noter que des faux-positifs peuvent être observés, après une vaccination par exemple. Des tests de détection rapides des anticorps peuvent être utilisés au sein de la clinique vétérinaire, mais ils présentent de moindres niveaux de sensibilité et spécificité. Des réactions croisées entre sérovars sont par ailleurs possibles en début d'évolution de la maladie. La leptospirose est donc bien diagnostiquée, mais il y a erreur sur le sérovar. Ce phénomène est davantage marqué en santé animale puisque les batteries de test comptent seulement 5 à 7 sérovars, contre 30 en médecine humaine. La détection du génome des leptospires par un test PCR est possible très précocement. L'ACVIM recommande de réaliser l'examen avant d'entamer un traitement antibiotique, à partir à la fois de prélèvements de sang et d'urine. Un résultat positif associé à une clinique évocatrice permettra de conclure à une leptospirose. La culture des leptospires sur sang et urine est plus facile aujourd'hui que dans le passé. Elle permet d'observe les spirochètes en 24 heures lorsqu'elles sont présentes. Toutefois, cette technique, assez délicate, est surtout réservée aux laboratoires de référence.
Outre des mesures de réanimation et de support, le traitement de la leptospirose passe par une antibiothérapie. L'ACVIM recommande la doxycycline par voie orale, à la dose de 5 mg/kg toutes les 12 h durant 2 semaines, afin d'éviter que les leptospires ne persistent dans les reins. En cas de vomissements ou si l'animal supporte mal cette molécule, le praticien prescrira auparavant une pénicilline par voie intra-veineuse, pour lutter contre la bactériémie (ampicilline 20-30 mg/kg, amoxicilline 20-30 mg/kg ou pénicilline G 25 000-40 000 U/kg, toutes les 6 à 8 h, voire toutes les 12 à 16 h en cas d'IRA de stade 4). Si le risque zoonotique ne peut pas complètement être écarté, les précautions habituellement prises au sein de la clinique suffisent généralement à le juguler. Si l'animal se trouve au domicile de ses propriétaires, ces derniers devront impérativement éviter tout contact avec l'urine de leur chien durant les premières 48 h de l'antibiothérapie per os. La doxycycline peut éventuellement être administrée aux congénères du chien malade, y compris aux chats. Des travaux supplémentaires sont toutefois nécessaires avant d'adopter systématiquement cette approche, prévient l'ACVIM.
La vaccination est conseillée chez le chien à partir de l'âge de 12 semaines. L'ACVIM recommande aux praticiens de connaître les sérogroupes présents dans la région où ils exercent afin de bien choisir leur vaccin. L'immunité conférée par la vaccination est en effet spécifique à un sérogroupe. Pour faciliter la prévention de la leptospirose, des vaccins quadrivalents sont aujourd'hui à disposition des vétérinaires (avec les sérovars Icterohaemorrhagiae, Canicola, Grippotyphosa et Australis en Europe). Si les chiens séjournant en groupe ou en chenil, ils devraient systématiquement être vaccinés : aucun chien n'est véritablement à l'abri, et ce quel que soit son mode de vie…
9 mai 2025
 5 min
5 min

7 mai 2025
 5 min
5 min

6 mai 2025
 5 min
5 min

5 mai 2025
 4 min
4 min
2 mai 2025
 5 min
5 min

30 avril 2025
 4 min
4 min
