26 avril 2024
 5 min
5 min
Bienvenue sur LeFil.vet
L'accès au site web nécessite d'être identifié.
Merci de saisir vos identifiants de connexion.
Indiquez votre email dans le champ ci-dessous.
Vous recevrez un email avec vos identifiants de connexion.

22 août 2019
Le cannabidiol, traitement adjuvant « prometteur » de l'épilepsie canine

Le cannabidiol administré par voie orale en plus du traitement classique de l'épilepsie idiopathique participe à une réduction du nombre de crises des chiens. Telle est la conclusion d'un essai randomisé conduit en aveugle sur un faible effectif de cas, par une clinicienne de la faculté vétérinaire de l'université du Colorado (USA). Pour l'auteure, cet adjuvant s'adresserait avant tout aux 20 à 30 % de cas d'épilepsie canine réfractaires à l'administration d'un anticonvulsivant reconnu.
Le cannabidiol est l'un des 104 cannabinoïdes identifiés dans la plante Cannabis sativa, et n'a pas d'effet psychotrope, contrairement au tétrahydrocannabinol. L'auteure a identifié des publications montrant l'effet anticonvulsivant du cannabidiol, sur des rongeurs de laboratoires dont les crises convulsives ont été provoquées. Mais – surtout –, une formulation « à base de 99 % de cannabidiol a été récemment approuvée par la FDA [en juin 2018] pour le traitement des formes résistantes [rares] de l'épilepsie chez l'Homme ». Pour lancer l'essai clinique, les auteurs ont posté une annonce de recrutement de cas sur le site web du service de neurologie de la faculté vétérinaire du Colorado. L'objectif était de recruter 30 cas au total.
Les cas étaient éligibles à inclusion dans l'étude s'ils présentaient, outre l'accord de leur maître :
Sur les deux années d'inclusion (2016 et 2017), 222 cas ont été évalués, et 90 % ont été rejetés du fait de l'exigence de ces critères : au final, 26 cas ont été inclus, dont 12 dans le groupe traité.
C'est un opérateur étranger au service de neurologie qui a tiré au sort les chiens pour leur inclusion au groupe traité ou placebo, et « ni les propriétaires ni les cliniciens ne connaissaient le statut des animaux » avant la fin de l'étude. Le traitement adjuvant concernait une administration orale biquotidienne de d'huile contenant du cannabidiol à 2,5 mg/kg (traitement) ou pas (placebo), sur 12 semaines. Les propriétaires notaient sur un formulaire dédié l'occurrence des crises épileptiques, leur type (une série de crises sur 24 h était noté comme un seul épisode) et leur durée, et revenaient en consultation toutes les 4 semaines pendant l'étude, pour prise de sang (mesure de la concentration sanguine en anticonvulsivants et paramètres biochimiques et hématologiques). L'hypothèse de travail était d'obtenir une réduction d'au moins 50 % de la fréquence mensuelle moyenne des crises. Un questionnaire sur la qualité de vie de l'animal (C-BARQ, comprenant une centaine de questions sur le comportement de leur animal) était rempli par les propriétaires au début et à la fin de l'essai. L'objectif était d'évaluer si le traitement avait un impact sur le comportement des sujets.
Seize chiens sont allés au bout des 12 semaines (dont 9 dans le groupe traité) ; onze avaient des crises généralisées (dont 6 du groupe traité) et les autres présentaient en plus des crises focales. Les auteurs observent bien une réduction significative de la fréquence des crises (voir le tableau ci-dessous), bien qu'elle soit inférieure au niveau attendu. Ils ne notent qu'une autre modification significative dans le groupe traité : une élévation des phosphatases alcalines (p=0,004) chez les 9 sujets du groupe. Toutefois, le faible effectif de l'étude et l'absence de dosage des acides biliaires (interactions médicamenteuses) empêchent les auteurs de conclure sur l'importance clinique de cet aspect. Il n'y avait aucune différence significative pour les données issues du questionnaire axé sur le comportement des chiens.
Effet du cannabidiol en traitement adjuvant de l'épilepsie au terme de 12 semaines d'essai clinique (LeFil, d'après McGrath et coll., 2019).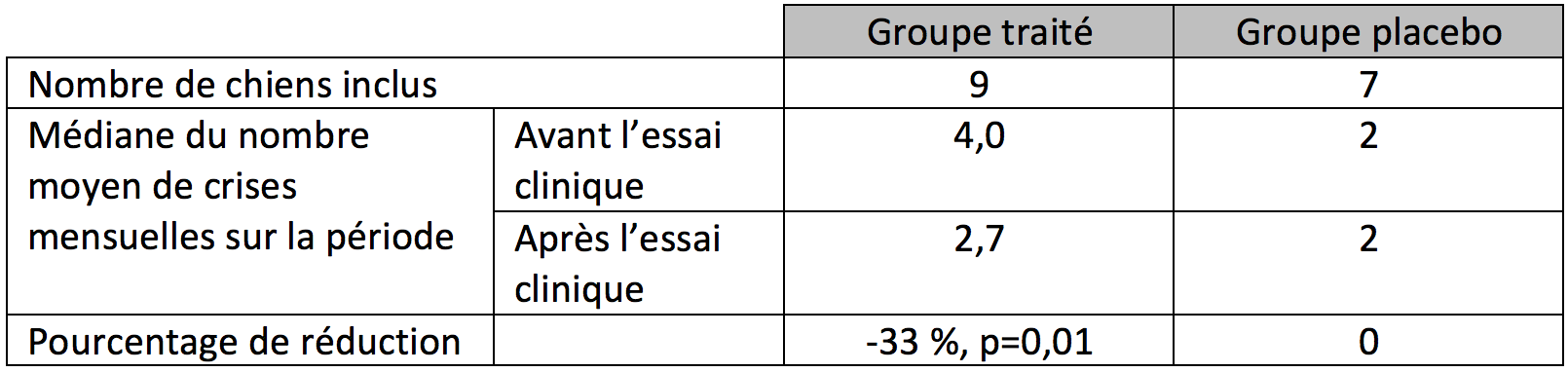
C'est un résultat « prometteur », même si, lorsqu'ils ne prennent en compte que les chiens “répondeurs” au traitement (50 % au moins de réduction des crises mensuelles), les auteurs en identifient 2 dans chaque groupe. Ils suggèrent qu'il faille adapter la dose administrée pour améliorer la réponse des autres sujets : « chez l'Homme, des données publiées depuis la fin de [leur] étude rapportent des posologies allant de 2 à 20 mg/kg/j ».
En compilant les valeurs des concentrations sanguines en cannabidiol (4, 8 et 12e semaines), les auteurs observent « une corrélation négative de la concentration plasmatique moyenne avec le pourcentage de changement par rapport à la semaine d'inclusion (r=-0,68, p=0,04) ». Pour les auteurs, cela confirme que la posologie choisie était probablement insuffisante ; ils proposent que « la prochaine étude repose sur un protocole avec dose croissante ».
En France, l'Agence nationale du médicament vétérinaire a récemment tenu à rappeler que les produits à base de cannabidiol présentés ou utilisés dans un but thérapeutique sont des médicaments vétérinaires (voir LeFil du 21 juin 2019). A ce jour, aucun médicament vétérinaire avec AMM est autorisé en France ou en Europe.
26 avril 2024
 5 min
5 min

25 avril 2024
 4 min
4 min

24 avril 2024
 4 min
4 min

23 avril 2024
 4 min
4 min

22 avril 2024
 4 min
4 min

19 avril 2024
 4 min
4 min