27 avril 2026
 3 min
3 min

Bienvenue sur LeFil.vet
L'accès au site web nécessite d'être identifié.
Merci de saisir vos identifiants de connexion.
Indiquez votre email dans le champ ci-dessous.
Vous recevrez un email avec vos identifiants de connexion.

10 février 2025
France : émergence d'un clone de staphylocoques dorés sensible à la méticilline chez les chats ; extension des SARM équins
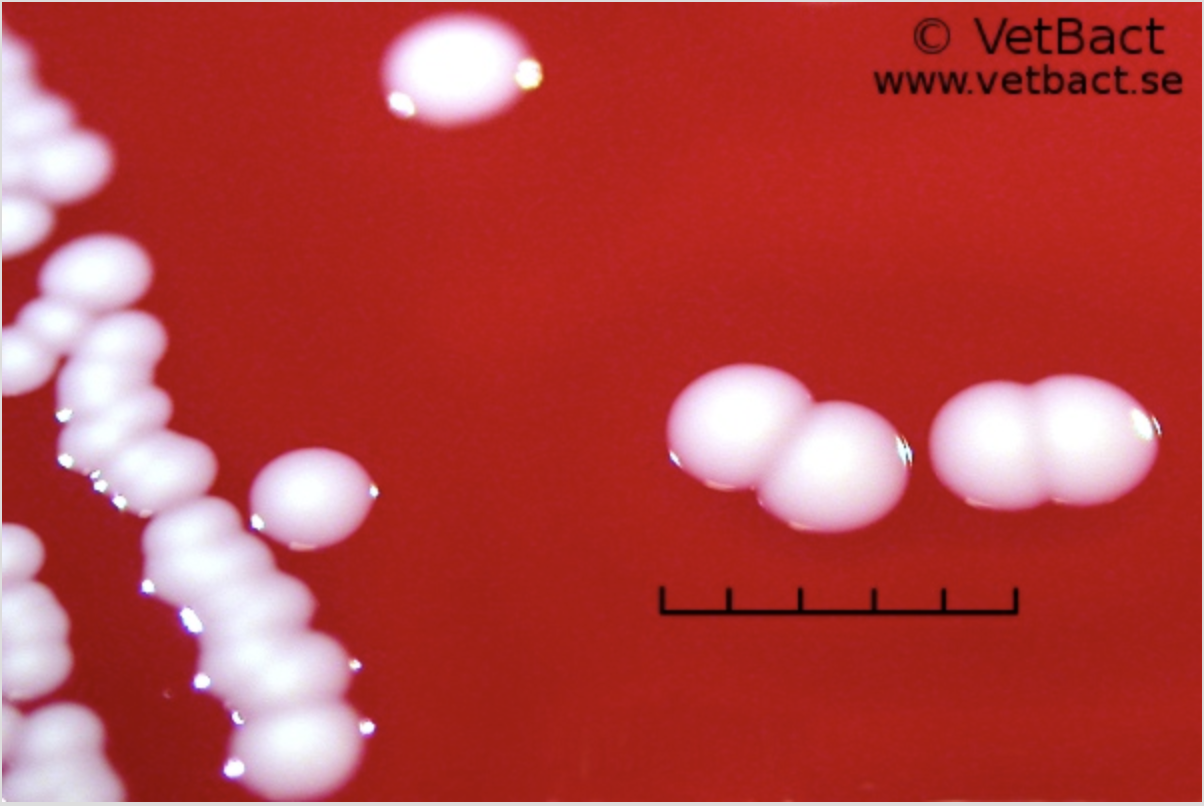

Le phénomène était brièvement rapporté dans le rapport 2023 du Résapath, publié fin 2024 : l'étude de souches félines de staphylocoque doré (Staphylococcus aureus) révèle l'importance d'un clone sensible à la méticilline, appartenant au groupe génétique CC398. Ce clone est à l'origine de bactériémies sévères chez l'humain. Une publication de début février vient fournir plus de détails sur cette émergence féline.
L'objectif initial était d'évaluer la présence de staphylocoques dorés résistants à la méticilline (SARM) chez les chiens, chats et chevaux en France, au travers d'isolats cliniques (infections cutanées, des tissus mous et respiratoires dans les trois espèces ; otites et infections urinaires chez les carnivores). Dans le cadre du Résapath, l'unité antibiorésistance et virulence bactériennes de l'Anses-Lyon a collecté auprès des laboratoires d'analyses les isolats obtenus en 2022-2023 sur l'ensemble du territoire, pour en déterminer l'éventuelle résistance à la méticilline (via la céfoxitine). La confirmation de ce phénotype était évaluée en PCR (recherche des gènes mecA et mecC).
Pour les chats, 14 des 186 isolats obtenus d'autant de patients ont été confirmés SARM, soit 7,5 % (ils comportaient tous le gène mecA sauf un isolat, mecC+). Si d'une manière générale ces SARM comportent plus de gène de résistance aux antibiotiques que les S. aureus sensibles à la méticilline (SASM), certains SARM ne comprenaient aucun ou un seul autre gène de résistance que le mecA ou mecC (qui confère une résistance à toutes les ß-lactamines vétérinaires). Bien que les SARM soient des pathogènes humains d'importance en santé publique – surtout à l'hôpital – les auteurs sont rassurants car cette prévalence de 7,5 % est stable par rapport à l'enquête précédente, de 2015. Et comme en 2015, les SARM présents sont à la fois des souches d'origine humaine (contamination probable des animaux par les maîtres) ou appartiennent au complexe clonal dit “du bétail”, le CC398 (noté ST398), qui est connu pour être bien adapté aux porcs, bovins, chevaux, ou au clone ST612. L'analyse génétique montre d'ailleurs que la plupart des SARM ST398 félins sont apparentés aux souches décrites initialement chez les porcs au Danemark.
En revanche, la “versions” sensible à la méticilline (SASM) du ST398 est considérée comme indépendante des animaux (elle représente la souche humaine “originelle”, avant son passage à l'animal, avec des adaptations génétiques). En santé humaine, elle peut provoquer des bactériémies sévères. Or l'originalité de cette étude est d'identifier que chez les chats, le SASM ST398 représente près du quart (24,8 %) des souches de staphylocoque doré non SARM (et 14,7 % des souches canines). Il semble que le chat puisse être suspecté de représenter un « réservoir préférentiel » pour ces SASM CC398. Les auteurs estiment que cela justifie d'explorer la « dynamique de la transmission du SASM ST398 entre les humains et leurs animaux » de compagnie. Pour les chiens, la proportion de SARM était plus faible, à 6,3 % des 143 chiens prélevés et les souches ST398 étaient apparentées aux lignées de SARM du cheval. Les auteurs relèvent d'ailleurs que c'est en apparente contradiction avec le fait que le mode de vie des chiens soit plus proche des chats que des chevaux… Ce qui mériterait d'être exploré plus en détail. Mais c'est le rôle des chats comme réservoir des SASM qui retient avant tout l'attention des experts.
Pour les chevaux, la proportion de SARM était de 28,7 % (à partir de 150 isolats). Ce qui inquiète le plus les auteurs de cette étude, c'est qu'en 2010, leur proportion n'était que de 10 %, soit un triplement en près de 12 ans… Ce « changement profond » est « potentiellement attribuable à l'émergence du clone ST612 », qui représente deux isolats de SARM sur trois, les autres étant des ST398. « Il est intéressant de noter que quatre chevaux [ST612+] provenaient du même élevage sur une période de trois mois, ce qui montre la capacité de ce clone à provoquer des épidémies locales ». À noter aussi que très peu (1,7 %) des souches de SARM équines sont associées directement à un SARM humain (mais les chevaux peuvent être source de colonisation des humains). Les auteurs relèvent aussi que trois isolats canins d'autant de départements étaient des ST612, « sans pouvoir vérifier s'ils avaient des contacts avec des chevaux ». L'analyse génétique de ces souches montre que leur origine est différente des ST612 s'étant transmis depuis l'Afrique du sud vers l'Australie et les USA. Sur la fréquence élevée des SARM en équine, les auteurs proposent que cela puisse, entre autres, être lié à « la présence de différents clones et plasmides porteurs de résistance, à des utilisations différentes des antibiotiques, à une plus grande contamination des cliniques équines par des bactéries multirésistantes, ou au fait que S. aureus n'est pas la principale espèce de Staphylococcus associée aux chiens et aux chats », présentant donc une prévalence moindre de SARM. Il reste aussi à comprendre « dans quelle mesure les isolats ST612 ont été disséminés en Europe. Ces données seront particulièrement importantes compte tenu du potentiel zoonotique de ce clone, qui est également souvent porteur de gènes de résistance multiples aux non β-lactamines » et de facteurs de virulence.
27 avril 2026
 3 min
3 min

24 avril 2026
 6 min
6 min

23 avril 2026
 4 min
4 min
22 avril 2026
 3 min
3 min

21 avril 2026
 5 min
5 min

20 avril 2026
 2 min
2 min