10 juin 2026
 3 min
3 min
Bienvenue sur LeFil.vet
L'accès au site web nécessite d'être identifié.
Merci de saisir vos identifiants de connexion.
Indiquez votre email dans le champ ci-dessous.
Vous recevrez un email avec vos identifiants de connexion.

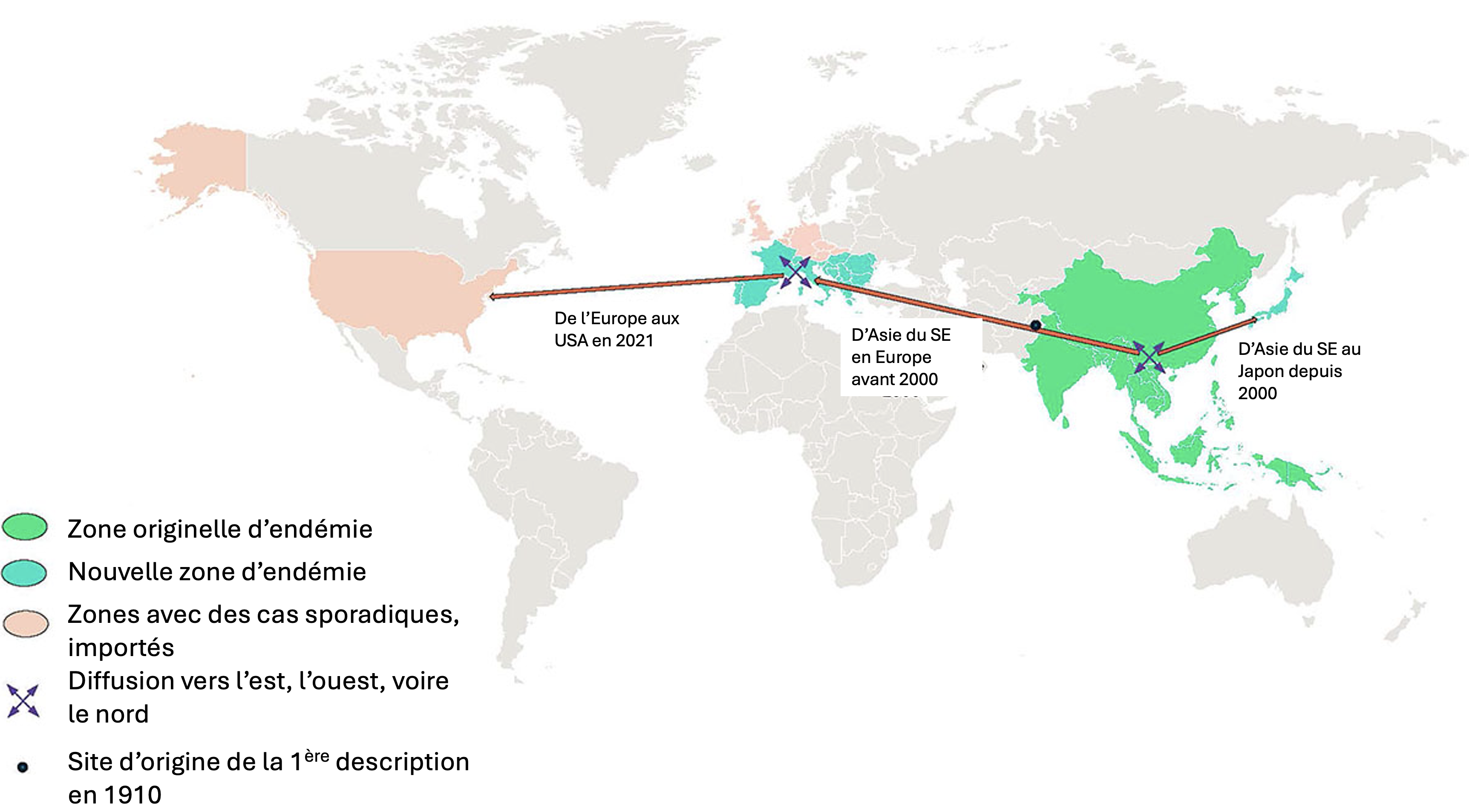
Sur les trois dernières décennies, Thelazia callipaeda, ver oculaire des carnivores pouvant passer à l'humain, a entamé et bien avancé son tour du monde. Originaire d'Asie du sud-est, il est parti en direction de l'ouest avant l'année 2000, et vers l'est à partir du nouveau millénaire.
Dans une revue de synthèse, des parasitologistes vétérinaires reviennent que la success-story de ce nématode, classé parmi les parasites internes bien que vivant avec un accès extérieur permanent : l'œil des carnivores (et parfois humain). Plus précisément, T. callipaeda vit pour l'essentiel à la surface de l'œil, dans les sacs conjonctivaux et les canaux lacrymaux. Son cycle est assuré avec l'aide d'un vecteur : « des mouches des fruits lacryphages du genre Phortica », proches des drosophiles. Chez un hôte infecté (chien, chat, renard, martre, raton-laveur, etc.), la mouche qui se nourrit des sécrétions oculaires (l'inflammation locale liée à la présence des vers adulte favorise ces sécrétions) va ingérer les larves L1. « À l'intérieur de la mouche, les larves se développent en larves infectieuses de troisième stade (L3) en deux à trois semaines environ. La mouche dépose ensuite les larves L3 sur l'œil d'un nouvel hôte définitif lors de son repas suivant. Les vers atteignent le stade adulte en un mois environ ». Le premier traitement sera l'extraction manuelle par un vétérinaire (anesthésie locale), et un relais préventif par lactones macrocycliques.
Ces auteurs soulignent que, « au cours des deux dernières décennies, [c'est devenu] un parasite zoonotique important en Europe, avec une aire de répartition géographique en expansion » (voir l'illustration principale). Initialement introduite au Piémont (Italie) en 1989, l'espèce « s'est ensuite propagée vers le nord et l'ouest, touchant la Suisse, la France et l'Espagne, puis les pays d'Europe de l'Est bordant la mer Adriatique. Elle est désormais implantée dans toute l'Europe, avec une augmentation des signalements dans de nombreux pays ». En France, en 2018, il était signalé en expansion dans le Sud-Ouest. Les auteurs signalent qu'il s'agit bien d'une diffusion depuis le point d'entrée italien car au plan génétique, il y a un groupe qui domine les vers collectés en Europe. Toutefois, « des analyses moléculaires récentes ont permis de détecter de nouveaux variants chez l'humain en Italie, suggérant soit une nouvelle introduction parasitaire, soit des mutations localisées ». Ils signalent aussi « des cas sporadiques récemment apparus aux États-Unis, en particulier dans la région de New York, généralement liés à des animaux importés », correspondant au génotype européen dominant.
La pathogénie de l'infection est rarement sévère : les vers, sur la surface oculaire, provoquent une « irritation mécanique continue [qui] perturbe l'intégrité épithéliale, créant des conditions propices à la persistance et à la reproduction du parasite ». Mais ce n'est généralement qu'à l'origine d'une gêne aiguë, « même en cas de faible charge parasitaire ». Deux réservoirs coexistent :
Le contrôle de l'infection est complexe car la seule prévention chez les carnivores domestiques ne suffit pas et peu de méthodes de luttes sont disponibles contre le vecteur… Pour les auteurs, « compte tenu de l'influence du changement climatique, de la mobilité animale et des facteurs environnementaux sur l'écologie vectorielle, des stratégies “Une Seule Santé” coordonnées seront essentielles pour limiter la propagation continue et l'impact zoonotique de ce ver oculaire émergent ».
10 juin 2026
 3 min
3 min

9 juin 2026
 5 min
5 min

8 juin 2026
 5 min
5 min

5 juin 2026
 3 min
3 min

4 juin 2026
 3 min
3 min
