24 avril 2024
 4 min
4 min

Bienvenue sur LeFil.vet
L'accès au site web nécessite d'être identifié.
Merci de saisir vos identifiants de connexion.
Indiquez votre email dans le champ ci-dessous.
Vous recevrez un email avec vos identifiants de connexion.

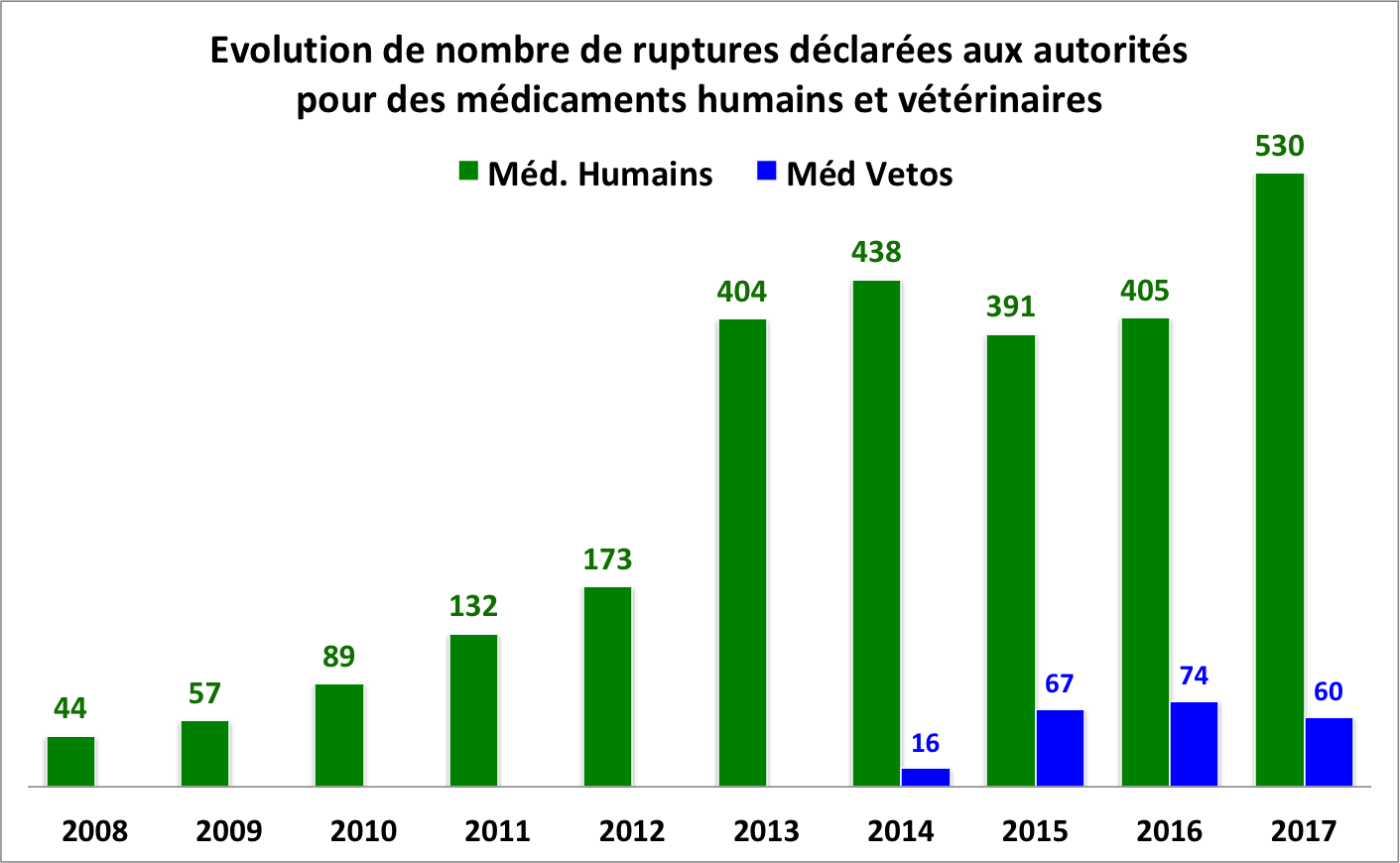
Les ruptures en médicaments ne touchent qu'environ 3 % des médicaments humains et, sans doute, une proportion similaire de médicaments vétérinaires. Même si cela peut paraître faible, le sujet est grave pour la santé humaine et animale. « Ces phénomènes le plus souvent diffus sont récurrents et fortement déstabilisateurs au quotidien », constatent une mission d'information conduite par deux sénateurs en 2018.
Il y a eu en 2017 plus de douze fois plus de ruptures déclarées qu'il y en avait en 2008 pour des médicaments humains. Et le record sera sans doute à nouveau battu en 2018. Pour les médicaments vétérinaires, les pénuries en centrales ont doublé depuis 2010.
Les ruptures et surtout les causes des ruptures démontrent que la France ne maîtrise pas du tout son approvisionnement de médicaments « majeurs », « essentiels » ou « critiques » pour la santé des populations françaises, humaines ou animales. Les vaccins et les antibiotiques dans les deux médecines, ainsi que les anticancéreux en médecine humaine, représentent les trois classes les plus fréquemment touchées par des ruptures. Ce sont donc des médicaments indispensables, incontournables, même pour la santé humaine ou animale.
En pharmacie vétérinaire, la moitié (46 %) des ruptures déclarées en 2017 à l'Agence du médicament vétérinaire affecte les vaccins, devant les antibiotiques (13 %). Mais en 2016, les ruptures en antibiotiques vétérinaires étaient aussi nombreuses que celles des vaccins, respectivement 39 % et 38 % des cas de ruptures déclarées à la même agence. En 2018, le nombre de lignes de médicaments humains en rupture dans les pharmacies a presque doublé par rapport à 2017, selon l'observatoire mis en place par l'Ordre des pharmaciens. Dans un CHU, près de 10 % des médicaments nécessaires aux soins hospitaliers sont en rupture au moins une fois dans l'année. Et dans 60 % des cas, la durée de la rupture a été plus longue qu'annoncée.
La mission d'information du Sénat s'inquiète, voire même s'alarme, de cette situation qui pourrait dégénérer en crise sanitaire s'il devenait impossible de soigner des patients ou des animaux faute de la disponibilité de médicaments dans l'hexagone. Car au fil des ans, petit à petit, la France, voire l'Europe et même les États-Unis, ont perdu leurs capacités de production de substances actives. Ce rapport est centré sur les médicaments humains. Mais ses constats et ses conclusions sont, pour la plupart, transposables aux médicaments vétérinaires.
Car, selon le rapport du Sénat, les premières causes de ruptures sont industrielles : les défauts de qualité de matières premières, la présence d'impuretés, le non-respect de normes environnementales qui conduisent à la fermeture de lignes de production dans des pays lointains, les incidents de production…
« Les patients français sont désormais dépendants d'industriels basés en Asie », constatent les deux sénateurs qui ont mené cette mission, et plus particulièrement dépendants d'industriels basés en Chine et en Inde. Dans les années quatre-vingt, 80 % des matières premières étaient produites en Europe. Trente ans plus tard, la proportion s'est inversée. 80 % des matières premières sont importées de pays asiatiques aussi lointains qu'incertains. Aujourd'hui, 53 % des substances actives pharmaceutiques sont produites en Chine et 22 % en Inde. De nombreuses substances actives ne sont d'ailleurs plus produites qu'en Chine ou en Inde et parfois que par un seul fournisseur. Ainsi, la fermeture d'une seule usine en Chine peut provoquer une pénurie mondiale de longue durée sur la pénicilline G. Inacceptable.
Par un simple « effet domino », la défaillance d'un site de production en amont sur une matière première d'un fournisseur conduit à une pénurie sur les autres sites de productions qui dépendent de ce fournisseur. Et les contraintes réglementaires des AMM ne permettent pas de substituer un fournisseur de matière première pharmaceutique par un autre, en quelques jours, ni même en quelques mois. Cela peut prendre un an ou plus avant que ce changement soit dans le dossier d'AMM puis accepté par les autorités.
Les multiples fusions-acquisitions ont conduit à ce que les usines soient de moins en moins nombreuses, de plus en plus spécialisées, et souvent délocalisées hors d'Europe pour couvrir un marché de plus en plus mondialisé. Ces usines sont moins flexibles et réactives que par le passé si les prévisions des ventes d'un pays comme la France se sont avérées insuffisantes. Surtout si le lointain marché français n'est plus considéré comme prioritaire. En outre, la défaillance d'un site ne peut plus être facilement compensée par un transfert de production sur un autre site. L'éloignement des sites de production hors de l'Union européenne nécessite aussi des contrôles à l'importation qui, retardent la libération des lots importés, voire l'interdisent en cas de non-conformité.
La mission d'information du Sénat émet donc 30 propositions « pour restaurer l'indépendance sanitaire de la France dans la production de ces médicaments, ce qui ne sera possible qu'à l'échelon européen ». Les sénateurs proposent de replacer « l'éthique au cœur de la chaîne de fabrication et de distribution des médicaments », face à des stratégies industrielles qui, nécessairement, privilégient la mondialisation les sites de production, ce qui conduit à leur délocalisation.
De nombreuses propositions visent donc d'abord à renforcer la coopération européenne sur les ruptures (recommandations n° 1, 2, 7, 26 à 30). Il convient de s'accorder sur des définitions communes de « ruptures », de « médicaments essentiels » et sur les listes de substances actives stratégiques pour la sécurité sanitaire (n° 1 et 2). Dans l'UE27, seulement trois pays, la France, la Roumanie et la Slovénie, ont déclaré avoir mis en place un dispositif légal pour pallier ou prévenir les ruptures de médicaments humains. L'Agence européenne du médicament devrait tenir compte du risque de pénuries dans la gestion des AMM et notamment dans les demandes de modifications d'AMM qui permettraient de les prévenir ou de les résoudre. Une base de données européenne des médicaments pourrait aussi faciliter les échanges de médicaments entre deux pays (n° 27 et 28).
En outre, une recommandation (n° 7) propose d'intégrer dans les inspections européennes des sites de fabrication, une vérification des capacités de production par rapport aux besoins afin de prévenir en amont sur des risques de pénuries.
Quatre propositions (n° 3 à 6) visent à inciter les industriels à implanter des sites de production pharmaceutiques en France, à travers des exonérations fiscales, d'aides de d'état ou des régions, des partenariats publics-privés, de fonds de soutien à l'industrie pharmaceutiques…
Pour quelques médicaments « critiques » ou de « niche », des établissements publics, comme la Pharmacie centrale des armées, pourraient être dotés des moyens de les produire ou de les importer d'autres pays en cas de défaillance des industriels (n° 8).
Les sénateurs reconnaissent aussi des causes économiques à certaines ruptures. La baisse régulière des prix des médicaments (humains) remboursés a conduit à rendre le marché français peu attractif par rapport à d'autres pays. Les industriels reconnaissent dans ce rapport ne pas privilégier le marché français dans les allocations de stocks. Néanmoins, des marchés plus rémunérateurs pour les industriels n'échappent pas non plus à des ruptures récurrentes. Le Sénat demande toutefois de prévoir une renégociation des prix avec les autorités sanitaires, lorsque des prix trop bas de médicaments conduisent les industriels à délaisser le marché français (n° 9).
En outre, les prix des médicaments étant plus bas en France que dans les autres pays d'Europe, des distributeurs se sont spécialisés dans les exportations parallèles vers d'autres pays de l'UE. Le Sénat propose alors de restreindre, contrôler voire empêcher et sanctionner ces exportations parallèles si cela est nécessaire (n° 17 à 19).
Le Sénat s'interroge aussi, voire condamne à demi-mot, la pratique commerciale des appels d'offres réalisés par les hôpitaux, qui s'apparente aux appels d'offres réalisés par les GIE. Car ces appels d'offres, de plus en plus gros en regroupant les demandes de plusieurs hôpitaux, ont « des effets pervers » en termes de ruptures. Cela conduit à une surenchère à la baisse — les remises obtenues par les appels d'offres peuvent atteindre 90 % du prix du médicament —. Au final, ces pratiques aboutissent à des situations de monopole pour le « moins-disant » et, par conséquent, à des situations de ruptures lorsque le moindre grain de sable perturbe sa chaîne de production et ne lui permet pas de fournir les volumes de médicaments prévus. Dans ce cas, il devient difficile de solliciter le fournisseur exclu de l'appel d'offres, qui, légitimement, n'avait pas anticipé ces commandes urgentes dans son planning de production. Le Sénat demande de mieux encadrer ces appels d'offres en limitant leurs volumes et en sécurisant davantage les approvisionnements (n° 10 et 11).
Pour responsabiliser davantage les industriels sur l'éthique de leurs missions, le Sénat demande que le site de l'Agence du médicament humain (ANSM) publie l'historique des ruptures de chaque laboratoire et leurs plans de gestion des pénuries (n° 12 et 13).
En outre, les laboratoires qui ne respectent pas leurs obligations « d'un approvisionnement approprié et continue » du marché français en médicaments essentiels devraient être sanctionnés avec une publication de ces sanctions sur le site de l'ANSM (n° 16).
Les sénateurs constatent que l'opacité des informations sur les ruptures conduit à un climat de méfiance entre les différents acteurs : les pharmaciens, les distributeurs et les industriels. La communication de l'Agence du médicament humain sur ce sujet est « très insuffisante ». En France, contrairement à d'autres pays européens, il n'est pas possible de disposer d'une liste actualisée au jour le jour des médicaments en rupture avec les mesures prises pour y faire face et avec une date suffisamment précise de réapprovisionnement.
Les sénateurs recommandent de mettre en place, sous la forme d'une base de données actualisée, « un partage de l'information exhaustif entre tous les acteurs » y compris entre les pharmaciens et les médecins-prescripteurs (n° 14 et 15). Les sénateurs estiment qu'une telle information devrait être accompagnée d'une grande vigilance pour éviter des comportements de « surstockage » sur des médicaments signalés en situation tendue.
Les sénateurs font cinq recommandations pour la faciliter la gestion des ruptures par les pharmacies d'officine (n° 20 à 24) :
24 avril 2024
 4 min
4 min

23 avril 2024
 4 min
4 min

22 avril 2024
 4 min
4 min

19 avril 2024
 4 min
4 min
18 avril 2024
 3 min
3 min

17 avril 2024
 4 min
4 min
