25 avril 2024
 4 min
4 min

Bienvenue sur LeFil.vet
L'accès au site web nécessite d'être identifié.
Merci de saisir vos identifiants de connexion.
Indiquez votre email dans le champ ci-dessous.
Vous recevrez un email avec vos identifiants de connexion.

Évaluer, à son retour de vacances dans une zone à risque de leishmaniose, si les mesures préventives vis-à-vis des phlébotomes ont été efficaces ou efficacement appliquées par le maître devrait être prochainement possible, grâce à un test rapide réalisable en consultation. En effet, un test immunochomatographique sur bandelette, visant à évaluer par la sérologie l'exposition d'un chien à la salive de Phlebotomus perniciosus, développé par une équipe belgo-tchèque, vient d'être décrit en détail dans une publication en libre accès.
Le test utilise comme antigène une protéine de la salive des phlébotomes, SP03B, produite par génie génétique (voir LeFil du 21 octobre 2016) et vise donc à détecter dans le sérum des chiens la présence d'anticorps (IgG) contre cet antigène. Si de tels anticorps sont présents, c'est bien que le chien a été exposé aux phlébotomes. D'autres espèces de phlébotomes sont impliquées dans la transmission de la leishmaniose canine (5 en tout), mais « P. perniciosus en est le principal vecteur sur le pourtour méditerranéen » et au-delà, comme le montre la carte de répartition européenne de l'espèce (voir ci-dessous).
La carte de répartition de P. perniciosus en Europe, mise à jour à mai 2018, est publiée par le centre européen de contrôle des maladies infectieuses (E-CDC).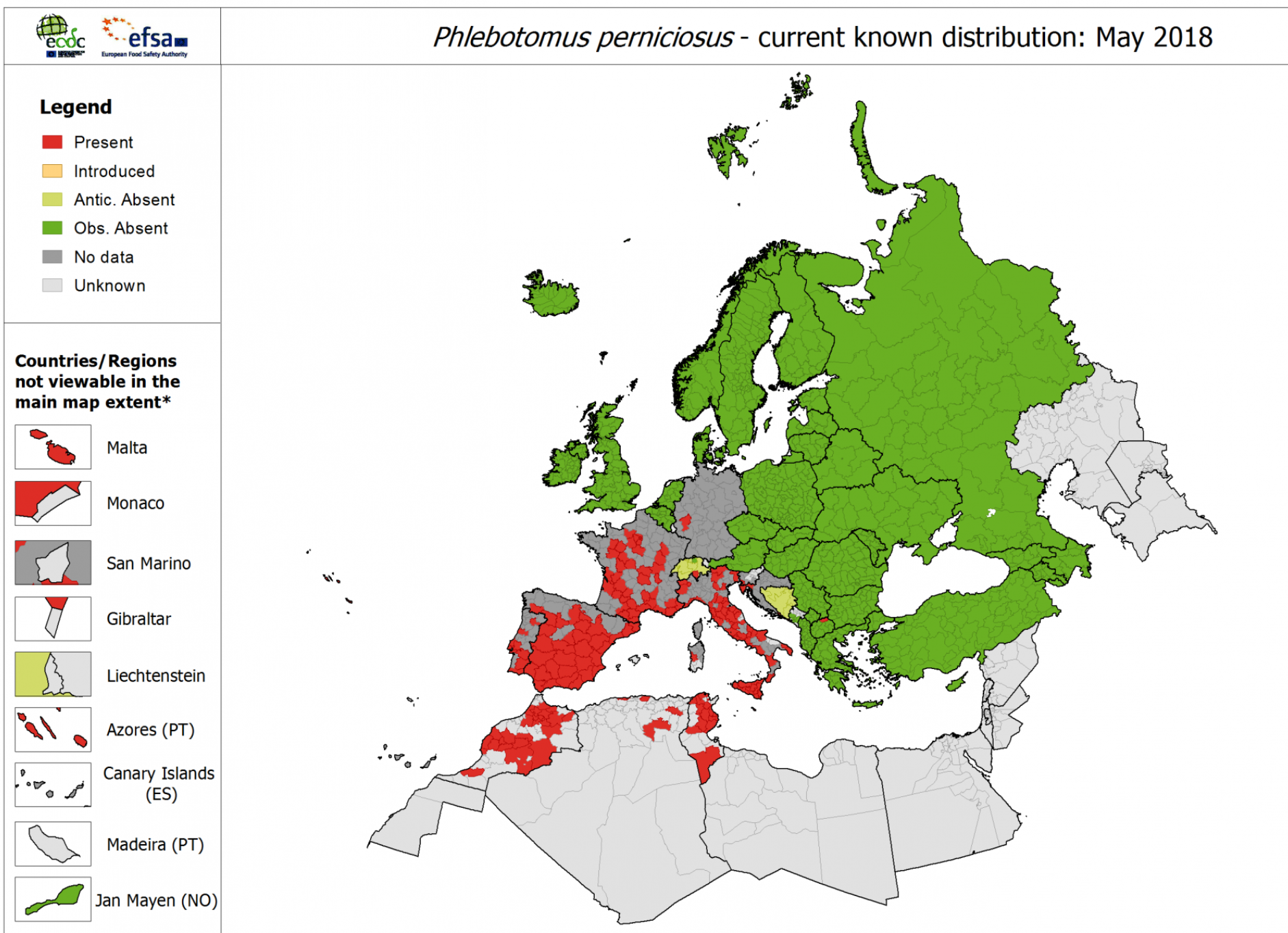
Dans une publication antérieure, la partie tchèque de cette équipe avait déjà vérifié que la concentration sérique en anticorps (IgG) anti-SP03B était corrélée à l'intensité de l'exposition aux piqûres de phlébotomes femelles, y compris pour des chiens naturellement exposés aux phlébotomes. Ce qui avait conduit au développement d'un test Elisa, dont la lourdeur ne permettait pas de le mettre à disposition des cliniciens en routine.
Pour évaluer ce test rapide, les auteurs ont utilisé du sérum prélevé sur des beagles, chiens d'expérimentation, ayant (n=42) ou non (29 d'Espagne et 24 du Nord de la France) été exposés à la piqûre de 200 phlébotomes. Ses performances ont été comparées à celles de deux Elisa indirects classiques, l'un utilisant du broyat de glande salivaire de P. perniciosus comme antigène, l'autre la protéine recombinante. À partir de ces échantillons, l'un des Elisa obtient 100 % de sensibilité, l'autre 69 %, tandis que le test rapide est lui aussi à 100 % de sensibilité. Pour la spécificité, les deux Elisa ont une même performance (98,1 %), tandis que la bandelette obtient 86,8 % de spécificité. Toutefois, pour ce résultat, les auteurs n'ont pris comme négatives que les bandelettes pour lesquelles aucune bande n'apparaît. Si une bande légèrement colorée sur la zone test est considérée comme négative, alors la spécificité du test remonte à 96,2 %. Comparé à la meilleure des deux méthodes Elisa, le test rapide présente un coefficient de corrélation (Kappa) de 0,83, ce qui signe une très bonne cohérence.
Les auteurs préviennent donc qu'avant de lancer leur test rapide, ils vont s'attacher à le valider sur un plus grand nombre de sérums de chiens piqués dans des conditions naturelles, et aussi évaluer son intérêt sur sang total. Ils préviennent aussi qu'il est en théorie possible que des anticorps dirigés contre les protéines salivaires d'autres espèces de phlébotomes du pourtour méditerranéen croisent pour leur test. Mais en l'absence d'élevage de ces espèces de phlébotomes, l'étendue de ces réactions croisées sera impossible à appréhender. Et comme ces espèces sont a priori elles aussi vectrices de la leishmaniose canine, cela ne devrait pas être de nature à modifier l'interprétation du test rapide.
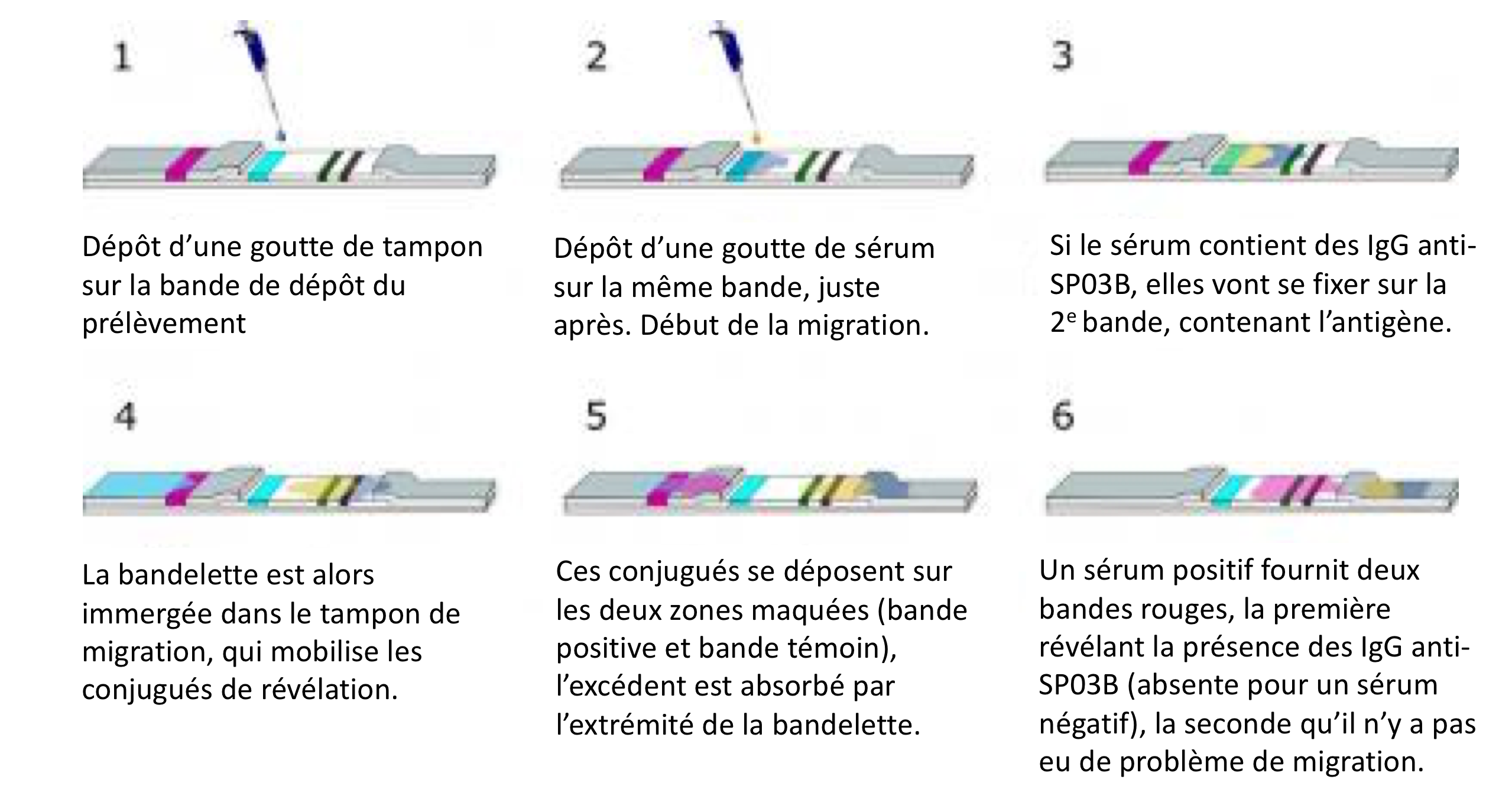
Les auteurs se sont donc orientés vers un test sur bandelette (immunochomatographique), mis au point avec une entreprise belge spécialisée dans le développement de tels tests, presque exclusivement en médecine humaine. Sur la bande “échantillon” de la bandelette du test rapide, il faut déposer une goutte de tampon juste avant d'y déposer le sérum à tester :
La zone de migration comportant ces trois bandes est en nitrocellulose et enchâssée de part et d'autre dans un support colloïdal comprenant deux conjugués :
La migration de ces conjugués ne commencera qu'après le dépôt du sérum à tester, lorsque l'opérateur trempera la bandelette dans la solution tampon. Le test réussit quand une bande (témoin, résultat négatif) ou deux bandes (témoin et SP03B, résultat positif) s'affichent, au terme de 15 minutes.
25 avril 2024
 4 min
4 min

24 avril 2024
 4 min
4 min

23 avril 2024
 4 min
4 min

22 avril 2024
 4 min
4 min

19 avril 2024
 4 min
4 min
18 avril 2024
 3 min
3 min
