19 avril 2024
 4 min
4 min
Bienvenue sur LeFil.vet
L'accès au site web nécessite d'être identifié.
Merci de saisir vos identifiants de connexion.
Indiquez votre email dans le champ ci-dessous.
Vous recevrez un email avec vos identifiants de connexion.

13 juin 2019
Dur dur d'être efficace ! Et surtout de le prouver. La médecine régénérative des tendinites bute sur les AMM

Boehringer Ingelheim lance actuellement le premier médicament équin avec AMM à base de cellules-souches, Arti-Cell° Forte, développé par la société belge Global Stem Cell Technology. Il s'agit du premier traitement de l'arthrose avec AMM issue de la médecine régénérative. Nous reviendrons dans un prochain Fil sur cette « première » de thérapeutique vétérinaire.
D'autres traitements de médecine régénérative, toujours en équine, n'ont, à l'inverse, pas réussi à satisfaire les exigences coûteuses des dossiers d'AMM pour des marchés qui restent étroits et économiquement limités par rapport aux mêmes produits utilisés en santé humaine. Ainsi, une entreprise parisienne, OTR3, spécialisée dans la médecine régénérative, vient de renoncer à sa demande d'AMM pour Equitend° déposée auprès de l'Agence européenne du médicament depuis janvier 2017.
Présentée comme un agent régénérant, cette solution injectable de poly-carboxy-méthyl glucose sulfate acétate (OTR4131), une sorte de polymère dérivé du dextran, avait été développée pour les chevaux atteints de tendinites en vue d'une injection locale dans le tendon lésé.
Face à l'insuffisance des données cliniques déposées en 2017, l'Agence européenne du médicament avait accordé un délai, jusqu'à la fin de l'année 2018, pour présenter un nouvel essai. Mais le coût et la durée de cette étude n'ont pas permis à OTR3 de le réaliser dans le délai fixé.
Sur son site (www.otr3.com), OTR3 se présente comme une « société innovante de développement de la thérapie matricielle en médecine régénérative avec une nouvelle classe d'agents thérapeutiques, les agents de régénération tissulaire ou RGTA (ReGeneraTing Agents) », dont ferait partie le poly-carboxy-méthyl glucose sulfate acétate.
En médecine humaine, OTR3 commercialise Calcipliq° 20 à base de la même substance régénérative, une sorte de kit de cicatrisation des ulcères chroniques fréquents chez les diabétiques. Ce kit entre dans la catégorie des dispositifs médicaux (comme un pansement) et non dans celle des médicaments à usage humain avec AMM. Son efficacité n'a donc pas été évaluée dans le cadre d'un dossier d'AMM par une autorité indépendante. Les dispositifs médicaux de médecine humaine bénéficient pour le moment d'un régime déclaratif assez souple auprès de l'agence du médicament humain.
De nombreux industriels préfèrent donc développer des produits comme des dispositifs médicaux, ce qui les dispense d'apporter aux agences du médicament les preuves d'efficacité préalablement à leurs ventes.
Il n'existe pas de catégorie légale de dispositif médical vétérinaire. Heureusement, cela n'interdit toutefois pas l'usage chez l'animal des pansements, des bandes, des implants, des thermomètres, des stéthoscopes, des seringues ou des aiguilles ou même des appareils de radiologie ou d'imagerie. Autant de produits ou de matériels inclus dans cette vaste catégorie des dispositifs médicaux en médecine humaine.
Avec l'abandon du dossier Equitend°, l'Agence européenne du médicament explique, dans son rapport public d'évaluation, les points forts mais aussi — surtout — les carences de ce médicament vétérinaire testé entre autres avec l'École vétérinaire d'Alfort, au Cirale de Dozulé (Calvados) et dans deux cliniques équines de Normandie.
Conditionné en flacon verre unidose d'un ml, la solution injectable à 10 mcg/ml de poly-carboxy-méthyl glucose sulfate acétate est destinée à être injectée localement « dans ou près des lésions des tendons fléchisseurs » sous contrôle échographique.
Pour l'agence européenne du médicament, le dossier qualité de la substance active, le poly-carboxy-méthyl glucose sulfate acétate, « n'est pas acceptable ». Les caractéristiques de la substance active ne sont pas constantes avec un impact clinique potentiel. Les contrôles qualité du produit sont déficients.
En revanche, la justification pharmacologique a été jugée acceptable. Toutefois, la plupart des études précliniques sont réalisées avec un composé proche, OTR4120, avec une extrapolation non démontrée de ces résultats à la substance active, OTR4131. La substitution de l'OTR4120 par l'OTR4131 n'est pas justifiée dans le dossier.
L'absence d'étude pharmacocinétique a été acceptée du fait que l'espèce de destination, les chevaux, est une espèce mineure.
La tolérance chez les chevaux traités est présumée bonne, mais pas bien étayée. Car les études cliniques présentent trop de carences pour bien évaluer cette tolérance (absence de collecte de données individuelles sur ce point).
Les chevaux visés sont exclus de la consommation humaine, ce qui élimine la nécessité d'évaluer les résidus et le temps d'attente.
Pour l'Agence européenne du médicament, « l'efficacité de Equitend° n'est pas démontrée ». La détermination de la dose efficace (1 ml, soit 10 mcg) apparaît mal étayée, sur des tout petits effectifs de chevaux : deux chevaux par dose testée ! L'étude de confirmation de cette dose « n'est pas considérée comme appropriée » avec 12 chevaux traités et un seul témoin. La portée de cette étude est seulement exploratoire.
L'étude terrain, randomisée et à l'aveugle, n'a inclus au final que 22 chevaux trotteurs français âgés de 4 à 7 ans, avec seulement 14 chevaux traités par Equitend° versus 8 trotteurs placebo (NaCl 0,9 %).
Selon l'agence du médicament, cet essai présente de nombreuses carences, surtout par le faible effectif. Malgré la randomisation à l'aveugle, les chevaux du groupe Equitend° sont affectés par des tendinites significativement plus sévères que celles du groupe placebo, tout du moins si l'on évalue la gravité de cette affection par l'étendue de la lésion : 1,70 cm2 versus 1,33 cm2. De ce fait, Equitend° permet de réduire l'étendue de la lésion aux alentours de 1,60 cm2 durant le suivi pendant 4 mois. Alors que l'étendue de la lésion reste, sans changement significatif, aux alentours de 1,33 cm2 dans le groupe placebo. Le traitement échoue donc à diminuer l'étendue de la lésion en dessous de celle du groupe placebo. À l'inverse, les chevaux traités Equitend° restent avec des lésions plus graves que celles du lot placebo. D'où le refus de l'agence européenne de considérer ce traitement comme efficace.
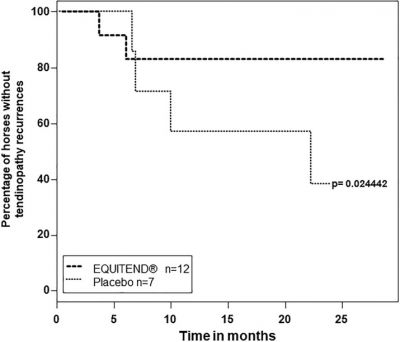
À l'inverse, les praticiens équins expérimentateurs jugent, dans leur publication de 2018, que l'efficacité de ce traitement est bien démontrée à travers les résultats suivants.
19 avril 2024
 4 min
4 min

18 avril 2024
 3 min
3 min

17 avril 2024
 4 min
4 min

16 avril 2024
 7 min
7 min

15 avril 2024
 5 min
5 min
12 avril 2024
 4 min
4 min