25 avril 2024
 4 min
4 min

Bienvenue sur LeFil.vet
L'accès au site web nécessite d'être identifié.
Merci de saisir vos identifiants de connexion.
Indiquez votre email dans le champ ci-dessous.
Vous recevrez un email avec vos identifiants de connexion.

14 septembre 2018
Retrait des AMM de la flunixine. Comment écouler les stocks ? Dans la légalité ? Ou pas !
La décision de suspendre les AMM de toutes les solutions injectables de flunixine prise le 26 juillet dernier n'était pas une vraie surprise pour les titulaires d'AMM (voir les Fils du 2 et 20 août 2018). Car, depuis le mois de janvier dernier, l'Agence européenne du médicament avait fait connaître d'abord ses doutes sur la cancérogénicité de son excipient, la diéthanolamine, avant de conclure, formellement fin juillet, à la nécessité de fixer une limite maximale de résidus pour cet excipient (voir LeFil du 30 août 2018).
Mais, la rapidité de la prise de cette décision de suspension d'AMM, prise sans préavis, en moins d'une semaine (entre le 20 et le 26 juillet), a par contre surpris. Car ni les laboratoires, ni les grossistes, ni, a fortiori, les praticiens n'avaient anticipé l'écoulement des stocks encore détenus par les fabricants, les centrales ou les vétérinaires, voire, dans certains cas les éleveurs.
Les décisions de suspensions d'AMM ont en effet été accompagnées d'un rappel de lots auprès des distributeurs en gros, mais pas auprès des ayants droit ou des éleveurs. Et vous êtes nombreux à vous interroger sur l'écoulement des stocks des ayants droit et même de ceux des éleveurs.
Est-il encore permis de détenir, prescrire, utiliser, vendre des médicaments dont les AMM ont été suspendues ? Et, si oui, dans quels délais ?
La législation nationale ou européenne sur les médicaments humains ou vétérinaires ne prévoit aucun délai pour l'écoulement des stocks dont les AMM sont modifiées (comme un temps d'attente allongé ou un changement de catégorie légale), suspendues ou retirées quelle qu'en soit la raison.
L'application stricte de la législation pharmaceutique devrait donc conduire au retrait immédiat de tous les stocks disponibles sur le marché, y compris ceux détenus par les ayants droit. Mais le risque pour la santé, humaine ou animale, de procéder ainsi avec autant d'urgence et de brutalité est, dans la majorité des cas, beaucoup plus élevé qu'une transition progressive et, si possible « indolore » pour les patients ou les animaux traités par des médicaments suspendus ou modifiés.
Le risque de ruptures induites sur les alternatives autorisées est aussi à prendre en compte, tout comme le délai nécessaire pour procéder à une substitution sur le terrain. Cette substitution ne peut matériellement pas être réalisée « du jour au lendemain ».
Il conviendrait donc de prévoir, à l'avenir, dans la législation, un encadrement des délais d'écoulement des stocks des médicaments suspendus ou modifiées. Malheureusement, ni la législation existante, ni le futur règlement européen « médicament vétérinaire » n'envisagent cela.
En pratique, une tolérance non écrite est souvent appliquée par les autorités d'inspection pour éviter de sanctionner inutilement et abusivement, l'écoulement de stocks qui ne sont pas devenus dangereux du jour au lendemain.
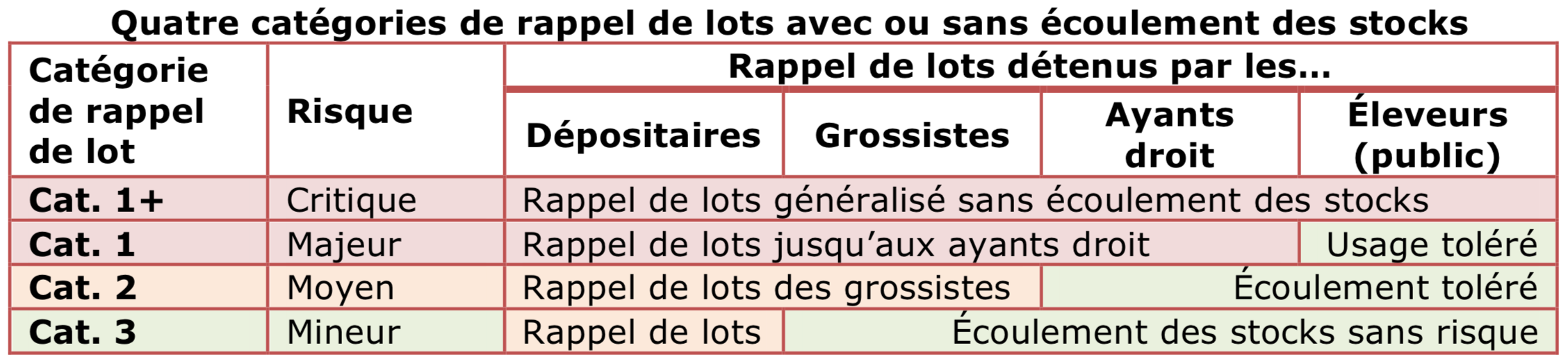
Le rappel de lot peut être considéré comme la base pour permettre ou non l'écoulement des stocks détenus par les grossistes, les ayants droit ou les éleveurs. Les autorités d'évaluation, en France, l'Agence du médicament vétérinaire (Anses-ANMV), peuvent ou non ordonner des rappels de lots des médicaments dont les AMM sont suspendues, retirées ou modifiées. L'Agence française classe ainsi les rappels de lots en quatre catégories :
Implicitement, si l'Agence décide d'un rappel de lot de catégorie 3, comme l'a décidé l'agence britannique pour les solutions injectables de flunixine, cela signifie que le risque pour la santé publique ou animale à écouler les stocks des centrales et des ayants droit n'est pas significatif.
L'Agence française a été un peu plus sévère que l'agence britannique pour ces mêmes médicaments à base de diéthanolamine. Elle a décidé un rappel de catégorie 2 auprès des dépositaires (les stocks qui appartiennent aux industriels) et des grossistes. Elle estime donc que l'écoulement des stocks des ayants droit ou leur usage par les éleveurs ne présente pas un risque supplémentaire pour la santé des consommateurs des résidus (éventuels) de cet excipient.
D'ailleurs, la diéthanolamine a été officiellement classée comme cancérogène possible (catégorie 2B) en 2013, il y a donc aujourd'hui cinq ans. Cela n'est que récemment, depuis la mi-janvier 2018, que les agences du médicament s'interrogent sur l'impact de ses éventuels résidus pour finalement conclure, qu'en l'absence de données, une toxicité des éventuels résidus ne pouvait pas être totalement exclue.
Les rappels de lots de catégories 2 ou 3 permettent de tolérer l'écoulement des stocks présents sur le terrain jusqu'à la fin de leur date de péremption. Car, si cela n'était pas tolérable, l'Agence a la possibilité d'étendre le rappel de lots auprès des ayants droit (rappel de catégorie 1), voire des éleveurs (catégorie 1+).
En Europe, certains États membres n'ont même pas encore commencé à suspendre les AMM. En outre, le Royaume-Uni a finalement décidé de conserver les solutions injectables de flunixine avec des indications restreintes aux équidés exclus de la consommation humaine.
Il est impossible de garantir qu'un inspecteur trop zélé prenne ce prétexte pour sanctionner un éleveur ou un vétérinaire qu'il aurait dans le collimateur. Néanmoins, si l'Agence décide de pas rappeler les stocks détenus par les ayants droit et les éleveurs, un inspecteur ne devrait pas reprocher l'écoulement des stocks puisqu'il est ainsi toléré par cette autorité. Même si cet inspecteur dispose bien des bases légales pour sanctionner tout à la fois la détention, la vente et l'usage d'une solution injectable de flunixine désormais interdite faute d'AMM.
Par conséquent, dans les abattoirs, il devrait toujours être accepté que des animaux traités par la flunixine même après le 26 juillet (date de la suspension des AMM), puissent être abattus sans être exclus de la consommation humaine (si le temps d'attente prévu est écoulé).
Cette tolérance devrait s'appliquer jusqu'à la fin de l'écoulement des stocks des ayants droit ou des éleveurs, soit, au maximum, jusqu'à la fin de la péremption de ces produits. Les stocks détenus par les ayants droit devraient évidemment rester en petites quantités. Il ne serait sans doute pas acceptable qu'un vétérinaire ou, a fortiori, un éleveur dispose d'un stock de flunixine injectable qui dépasse la fin de l'année 2018.
L'approche est évidemment contestable en droit. Car il pourrait être argué qu'il est interdit d'administrer un médicament dont les LMR des « substances pharmacologiquement actives » n'ont pas été fixées. Toutefois, il pourrait aussi être répliqué qu'un excipient comme la diéthanolamine n'est pas une « substance pharmacologiquement active ». Seuls des tribunaux pourraient trancher ce point de droit.
Néanmoins, cette approche pragmatique est la seule compatible avec un rappel de lots de catégorie 2 ou 3 qui tolère l'écoulement des stocks chez les ayants droit et les éleveurs.
De même, lors des inspections pharmacie, il est difficile de reprocher à un vétérinaire ou un éleveur de détenir des stocks (non périmés) de médicaments suspendus (ou modifiés) si aucun rappel de lot auprès des ayants droit et des éleveurs n'a intentionnellement été organisé.
Dans l'idéal (?), il conviendrait surtout de prévoir à l'avenir dans la réglementation pharmaceutique un encadrement sur des périodes d'écoulement des stocks de quelques mois, en s'inspirant par exemple du dispositif existant pour les biocides ou les aliments pour animaux.
Malheureusement, le projet de règlement européen sur le médicament vétérinaire en cours d'adoption est encore muet sur ce point. Et il faudra encore jongler pendant plusieurs années entre rigueur, pragmatisme et tolérance, parfois au mépris du droit.
25 avril 2024
 4 min
4 min

24 avril 2024
 4 min
4 min

23 avril 2024
 4 min
4 min

22 avril 2024
 4 min
4 min

19 avril 2024
 4 min
4 min
18 avril 2024
 3 min
3 min
